原发性胆道胆管炎(PBC)是一种慢性自身免疫性肝病,以进行性肝内小胆管损伤和抗线粒体抗体(AMA)升高为特征。这种疾病的发病机制涉及对线粒体丙酮酸脱氢酶复合物(PDC-E2) E2亚基的耐受性丧失和胆道上皮细胞(BECs)的自身免疫性损伤,导致胆汁淤积和进行性肝纤维化。
肝脏中CD4+ T和CD8+ T细胞浸润增加,提示异常活化的T细胞参与了BEC的凋亡。然而,免疫失调的机制仍有待确定潜在的治疗策略。大约20-40%的PBC患者对熊去氧胆酸(UDCA)没有完全反应,UDCA是目前批准用于治疗PBC的一线药物。之前开发并优化了几种PBC小鼠模型来研究致病性免疫细胞亚群,并确定了CD8+ T细胞在胆道病理发展中的关键作用。
肝脏包含一个特定的免疫微环境,其中有高比例的常驻免疫细胞,包括组织常驻记忆CD8+ T细胞(Trm)。CD8 + Trm细胞是一种特殊的亚群,主要存在于非淋巴组织中,作为第一道防线,并在病原体再次攻击时迅速作出反应。
大多数关于CD8+ Trm细胞的研究都集中在它们对病原体的免疫作用上。然而,CD8+ Trm细胞在许多自身免疫性疾病中也应答自身抗原并介导自身免疫。它们在PBC中的作用还有待进一步研究。

图片来源:https://doi.org/10.1038/s41467-024-46654-5
近日,来自华南理工大学的研究者们在Nature Communications杂志上发表了题为“Targeting pathogenic CD8+ tissue-resident T cells with chimeric antigen receptor therapy in murine autoimmune cholangitis”的文章,该研究揭示了嵌合抗原受体靶向致病性CD8+组织驻留T细胞治疗小鼠自身免疫性胆管炎。
原发性胆道胆管炎(PBC)是一种胆汁淤积性自身免疫性肝病,以自身反应性T细胞对肝内小胆管的反应为特征。在本研究中,研究者使用Il12b-/- il2ra -/-小鼠(DKO小鼠)作为自身免疫性胆管炎模型,并证明Cd8a敲除或用antid8α抗体治疗可以预防/减少胆道免疫病理。
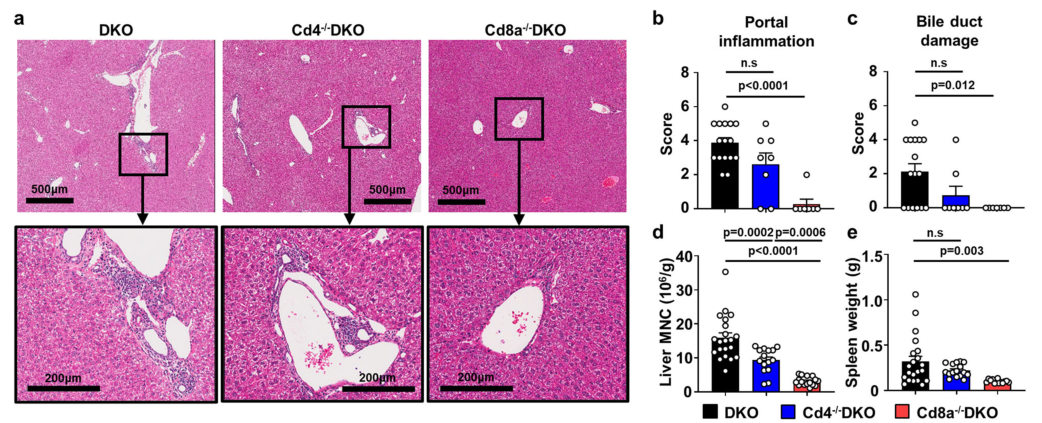
CD8+ T细胞在小鼠自身免疫性胆管炎中占主导地位,而不是CD4+ T细胞
图片来源:https://doi.org/10.1038/s41467-024-46654-5
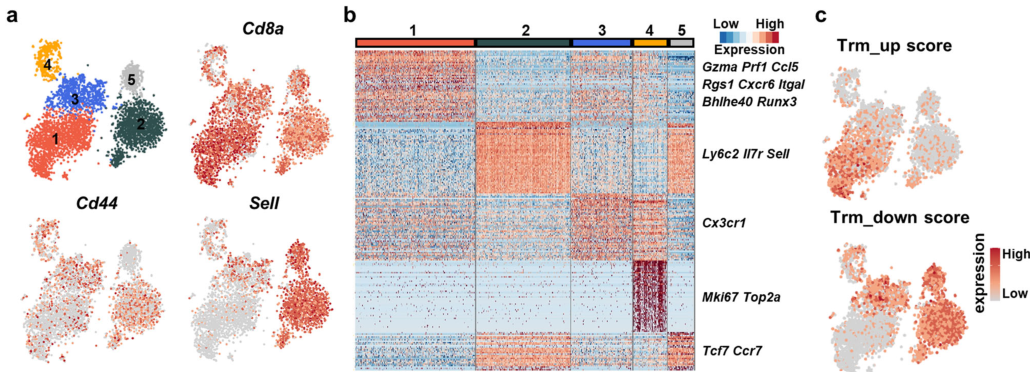
通过单细胞RNA测序分析,研究者在DKO小鼠肝脏中鉴定出CD8+组织驻留记忆T (Trm)细胞,这些细胞高度表达激活和细胞毒性相关标志物,并诱导胆管上皮细胞凋亡。肝脏CD8+ Trm细胞也上调几种免疫检查点分子的表达,包括PD-1。
研究者描述了靶向pd -1表达CD8+ Trm细胞的嵌合抗原受体的发展。pd -1靶向CAR-T细胞治疗DKO小鼠选择性地耗尽肝脏CD8+ Trm细胞并减轻自身免疫性胆管炎。本研究的工作强调了CD8+ Trm细胞的致病作用和pd -1靶向CAR-T细胞的潜在治疗用途。
DKO小鼠肝脏组织驻留记忆CD8+ T细胞的积累
图片来源:https://doi.org/10.1038/s41467-024-46654-5
最后,pd -1靶向CAR-T细胞可能应用于其他自身免疫性疾病,因为在小鼠模型中发现pd -1消耗抗体可以改善1型糖尿病和多发性硬化症。尽管耗尽型抗体在临床应用上要便宜得多,但由于二级淋巴器官中靶细胞的不完全耗尽,它们面临着复发等问题。然而,CAR - T细胞可以清除外周血和次级淋巴器官内的靶细胞。
此外,CAR-T细胞可以在宿主体内持续很长时间进行监测,并诱导患者持续无药缓解。因此,靶向PD-1的CAR-T细胞治疗为可能抵抗PD-1消耗抗体治疗的患者提供了一种策略。