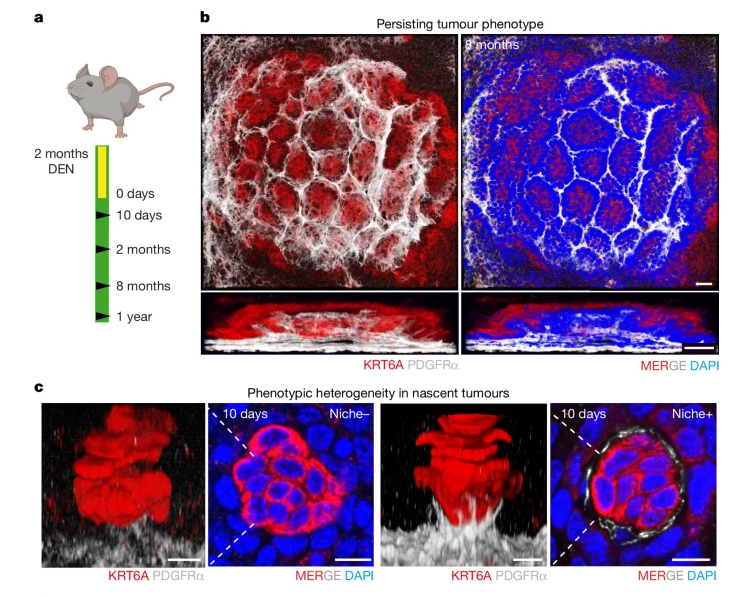
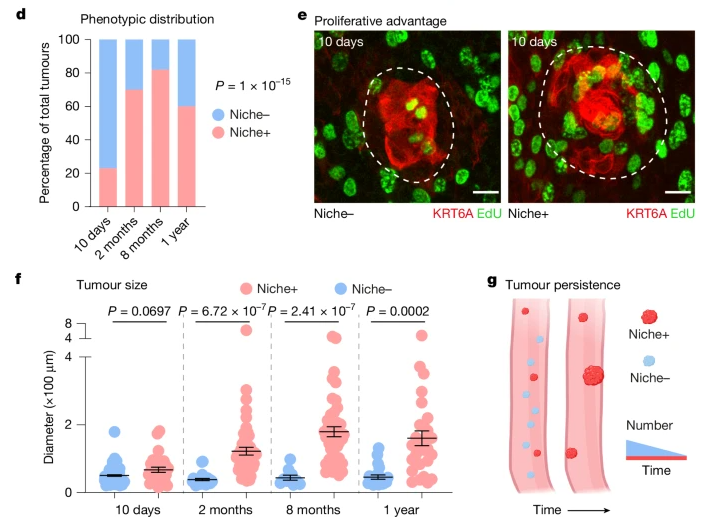
癌前生境重塑与肿瘤的长期存在密切相关
更令人震惊的发现是,癌前生态位本身就具备强大的促癌能力。研究人员通过功能性异质性 3D 培养实验和体内移植实验,将无致癌物暴露的健康上皮细胞与肿瘤来源的基质(即癌前生态位)共同培养或移植到免疫缺陷小鼠体内,结果发现,原本安分守己、无任何基因突变的健康上皮细胞,竟然也表现出了肿瘤的特征,不仅形成了类似肿瘤的形态,还出现了高度增殖的现象。
这一结果彻底颠覆了传统认知:过去我们始终将目光锁定在突变细胞本身,认为基因突变是癌症发生的唯一始作俑者,但这项研究明确证实,即便没有基因突变,一个被重塑的畸形微环境,本身就足以 “教唆” 正常细胞走上癌变之路。肿瘤的命运从来都不是突变细胞的 “独角戏”,而是突变细胞与周围正常组织的 “双向奔赴”——突变细胞是开启癌变的主角,但周围正常组织的反应,是围剿清除还是纵容庇护,直接决定了早期肿瘤能否存活并发展。
为了进一步厘清癌前生态位的形成机制,研究人员对其细胞组成和调控通路进行了深入解析。
结果发现,构成癌前生态位的核心细胞是黏膜固有层中的 PDGFRαⁿᵒʷ成纤维细胞,这类细胞在接收到肿瘤细胞的信号后会发生克隆扩增,且在肿瘤早期阶段,这些成纤维细胞并未表现出完整的癌症相关成纤维细胞(CAF)表型,仅处于前 CAF 的过渡状态,这也意味着癌前生态位的形成是肿瘤发生的极早期事件。
同时,研究还发现,免疫细胞和内皮细胞在肿瘤早期的生态位中几乎不存在,也不会对 Niche+(有生态位)和 Niche-(无生态位)肿瘤产生选择性作用,说明免疫反应并非早期肿瘤存活的关键因素。而在分子调控层面,研究人员鉴定出了调控癌前生态位形成的核心信号轴——EGF–SOX9–FN1 轴:早期肿瘤中高表达 SOX9 的上皮细胞,会通过分泌 EGF 家族配体(如 AREG)激活下方成纤维细胞的 EGFR 信号,诱导成纤维细胞向肿瘤迁移并大量分泌纤维连接蛋白(FN1),进而形成纤维化的癌前生态位;而这个生态位又会反过来通过细胞外基质的相互作用,持续促进肿瘤细胞的增殖,形成一个促癌的正反馈循环。
当研究人员通过实验阻断这一核心信号轴时,癌前生态位的形成被显著抑制:使用吉非替尼抑制 EGFR 信号,或用 FUD 肽抑制纤维连接蛋白的纤丝形成,都能让小鼠体内的 Niche+ 肿瘤数量大幅减少,绝大多数早期肿瘤因失去保护而无法存活,整体肿瘤负荷也显著降低。这一结果为癌症的早期干预提供了全新的思路:不必等到肿瘤发生基因突变或进展到中晚期,只需干扰肿瘤细胞与周围成纤维细胞之间的 “秘密对话”,阻断癌前生态位的形成,就能在癌症真正扎根之前,将其扼杀在摇篮里。而这一发现对于食管癌这类早期诊断困难的癌症来说,更是具有划时代的意义。
研究团队还在人类早期食管癌样本中完成了关键验证,无论是未经化疗的早期食管鳞状细胞癌(Tis、T1a、T1b),还是化疗后残留的异型增生组织,都观察到了与小鼠模型一致的特征:肿瘤细胞中存在异质性表达的 SOX9 和 AREG,且这些细胞周围有 PDGFRα+ 成纤维细胞的聚集和纤维连接蛋白的大量沉积,形成了与小鼠模型相似的癌前生态位。这一结果证实,癌前生态位的重塑并非小鼠模型中的特殊现象,而是人类食管癌早期发生的普遍机制,也为人类食管癌的早期诊断提供了潜在的生物标志物,为开发针对性的早期干预药物奠定了基础。
这项研究让我们重新认识了癌症发生的早期过程:正常组织并非被动等待癌细胞侵犯的受害者,从肿瘤刚刚冒头的那一刻起,它们就通过与突变细胞的相互作用,成为了癌症命运的共同书写者。这也解释了为什么有些人体内携带致癌突变,却能终生不患癌——他们的正常组织并未对突变细胞产生 “纵容”,没有形成促癌的癌前生态位,突变细胞最终被身体的正常调控机制清除。而研究发现的 EGF–SOX9–FN1 信号轴,以及癌前生态位这一全新靶点,为癌症的早期预防和干预开辟了新的方向。
目前,这项研究的临床转化虽仍处于早期阶段,但它已经为我们描绘了一幅全新的防癌图景:对抗癌症,不必等到它攻城略地,只需在它刚刚冒头、还在向周围组织 “求救” 的那一刻,切断它的信号传递,破坏它的 “保护舱”,就能从源头上阻止癌症的发生。这一发现不仅为食管癌,也为其他上皮源性肿瘤的早期研究和干预,提供了全新的范式和思路。